Nature一篇6000字「RNAi疗法」报告
RNA滋扰(RNAi)疗法的成长始于1998年颁发在Nature杂志上的一篇题为“Potent and specific genetic interference by double-stranded RNA in Caenorhabditis elegans”紧张论文。Andrew Fire、Craig C. Mello等科学家发现,使用长双链RNA (dsRNA)可以或许缄默奇丽隐杆线虫中特定基因的表达。
在该研讨的根基上,Thomas Tuschl等在2001年颁发的另一篇Nature论文中揭示,使用小滋扰RNA(small-interfering RNAs,siRNAs)在哺乳动物细胞中实现了序列特异性RNAi,且不会诱导使用长双链RNA (dsRNA)激发的免疫反响。基于这些紧张发现,siRNA在科研及治疗范畴的利用开端成长。
起源:Nature Biotechnology
与单链反义寡核苷酸(antisense oligonucleotides,ASO)分歧,siRNA是短的双链RNA (dsRNA),由一条与靶RNA具有雷同序列的公理链,及一条互补领导(反义)链构成。在被细胞摄取后,siRNA与RNA诱导缄默复合物(RISC,一个由AGO2内切酶、反式激活应答RNA联合卵白2和DICER1构成的多卵白体系)互相作用,公理链被肃清,领导链(反义链)充任辨认靶序列的模板,介导互补靶mRNA的联合及降解,从而终止靶卵白的翻译。
反义寡核苷酸(ASO)是首个获监管部分同意的寡核苷酸药物,合成ASO可以被设计成靶向剪接旌旗灯号序列并调节pre-mRNA剪接(图1a),也可以被设计成联合靶mRNA中的互补序列,并招募核糖核酸酶H1 (RNase H1)以降解靶mRNA(图1b)。外源性siRNA是内源性miRNA的“表亲”,应用siRNA诱导缄默复合物(siRISC)介导基因缄默(图1c)。miRNA应用miRNA诱导缄默复合物(miRISC)经由过程使mRNA脱帽或缩短poly(A)尾巴介导基因缄默(图1d)。(起源:Nature Biotechnology)
今朝,环球已有6款RNAi药物获批上市,验证了RNAi疗法在人类中的利用。跟着RNAi赓续取得治疗突破,该赛道的财产热度也在急剧上升。2023年以来,制药巨擘BD之风也吹到了RNAi范畴,罗氏牵手Alnylam(潜在生意业务总额28亿美元)、BI牵手瑞博生物(潜在生意业务总额超20亿美元)、诺华牵手舶望制药(潜在生意业务总额41.65亿美元)……MNC已绝不粉饰对RNAi疗法的兴致。此外,从管线来看,医药魔方NextPharma®数据库显示,截至2024年7月26日,环球有超620个RNAi项目同步在研。
已获批上市的RNAi疗法
起源:Nature Biotechnology
RNAi疗法具有特异性缄默险些任何治疗靶点的潜力。然而,将这类立异性疗法带给更多患者仍面对伟大的挑战,此中递送问题最为凸起。曩昔几年,RNAi疗法递送技术进展若何。RNAi疗法的靶点选择有何讲求。临床开发有哪些注意点。将来的上风成长偏向在哪。近日,来自University of Massachusetts Chan Medical School的两位科学家在Nature Reviews Drug Discovery 杂志颁发一篇综述文章,就以上问题睁开了深刻探究。
起源: Nature Reviews Drug Discovery
递送突破
siRNA向靶组织或细胞类型的功效性递送受到多种因素的影响,包含给药道路、生物屏蔽、外渗、组织或细胞摄取和内体逃逸。今朝获批用于递送siRNA的技术包含LNP和基于GalNAc的偶联技术(肝脏递送)。此中,偶联介导的递送是今朝临床上递送siRNA的主要平台。在LNP和GalNAc介导肝脏递送取得胜利后,今朝得当递送的组织正在扩展。此中,中枢神经体系(CNS)、眼睛、肺、肌肉和皮肤递送显示出可喜的进展,其他组织(包含肾脏、心脏、脂肪、胎盘和胰腺等)的递送也正在积极摸索中。这些提高主要归因于比来递送平台和给药模式的立异。例如,经由过程局部给药(local administration)可将siRNA选择性递送至中枢神经体系(CNS)、眼睛、肺和皮肤;经由过程体系递送(systemic delivery)可以使siRNA达到肌肉、肾脏、心脏、脂肪、胎盘和胰腺,固然这种办法没有选择性,但siRNA在可接受的剂量程度下会优先在这些组织中的某些细胞类型中积聚。
在分歧组织中实现治疗性RNAi递送的技术
起源: Nature Reviews Drug Discovery
▌体系性递送
偶联介导的递送
GalNAc偶联siRNA联合细胞外面去唾液酸糖卵白受体(ASGPR),经由过程内吞作用,匆匆进肝细胞摄取。已获批上市的6款RNAi疗法有5款使用了GalNAc体系。GalNAc介导的肝细胞递送是一种奇特的环境,肝脏的自然过滤功效、高血流量、开窗内皮以及ASGPR的快速轮回配合导致了壮大的疗效和持久性。今朝,一些靶向偶联物,包含抗体、工程卵白、肽、适体和脂质,正在开发用于siRNA肝外递送(图2a)。
肝外递送
转变药代动力学特性以改善siRNA全成分布和匆匆进肝外疗效的策略(起源:Nature Reviews Drug Discovery )
siRNA向非肝组织的体系递送在观点上是繁杂的,必要更好地舆解驱动肃清和生物散布的原理。siRNA的生物散布可能受到给药道路、核酸酶稳固性和肃清器官心理特征的影响。肝脏和肾脏是体系打针siRNA的主要肃清器。肝脏较高的血流速度、不持续的内皮以及肾脏的自然过滤功效会在到达充分的体系积聚之前就肃清年夜部门注入的化合物。
一样平常来说,骨架(scaffold)的整体亲疏水比决议了siRNA的肃清模式。高疏水性siRNA在肝脏中被肃清较多,高亲水性siRNA在肾脏中被过滤较多。事实上,与肌肉和中枢神经体系等组织(通常1–2 μg g−1就足够了)相比,肾脏中的靶向缄默必要高近两个数目级的siRNA积聚(>100 μg g−1)。是以,对付肾脏,必要额外的化学改革,如加强稳固性和内体逃逸,以进步疗效。肾脏是很多肾脏疾病的紧张器官,siRNA胜利递送到肾小球内皮细胞和足细胞等细胞类型,将开启前所未有的机遇。
有研讨显示,脂质偶联物(如docosanoic acid,phosphocholine (PC)–DCA)可以或许明显改善了siRNA的体系散布,在包含肌肉、心脏和脂肪在内的几种肝外组织中显示出疗效。除了表示出更好的肝外摄取外,这类化合物还显出更好的平安性。一项治疗先兆子痫的I期临床实验正在评估PC–DCA偶联siRNA对sFLT1的调节作用。此外,2′-O-hexadecyl (C16)脂质偶联siRNA正在临床前和临床研讨中被普遍评估。
显示出壮大体系肝外效用的其他类型偶联物包含抗体、抗体片断和工程卵白。这类偶联同时明显增长了siRNA药物的总体年夜小,从而经由过程低落肾脏肃清率匆匆进体系散布。
抗体偶联siRNA进展最快的是使用靶向转铁卵白受体1 (TfR1)的单抗,可用于骨骼、心脏和腻滑肌递送。在一项临床前研讨中,靶向SSB mRNA(编码小RNA联合外切酶掩护因子La),单次静脉打针6 mg kg - 1剂量的anti-TfR1–siRNA偶联物导致高达75%的靶点下调。一项针对人类患者的I/II期研讨注解,使用anti-TfR1–siRNA靶向肌张力卵白激酶(DMPK)治疗1型强直性肌养分不良,可明显改善疾病预后。
Centyrins是一类小的,工程化的人类卵白质衍生物,也被用于siRNA肝外递送。centyrin-siRNA偶联平台显示出有愿望的体系递送特征。一项使用centycin -conjugated siRNA (ABX1100)用于肌肉递送,以缄默糖原合成酶1 (GYS1)基因以治疗庞贝病的I期实验正在进行中。
肽偶联也有望成长为siRNA的递送平台。肽可以合成,是以CMC相对不那么繁杂。胰高血糖素样肽1(GLP1)是GLP1受体的一种配体,已被胜利地用于将ASO递送到胰岛细胞。很多学术试验室和制药公司正在进一步摸索肽偶联作为一种有出路的siRNA递送策略的潜力。
适配体是第一批被摸索用于递送siRNA和其他寡核苷酸疗法的偶联物之一,但可能因为早期的一些测验考试察看到的持久性有限,今朝还没有在转化范畴得到太多的存眷。不外,比来适配体在疾病动物模子中取得了明显进展,分外是靶向肿瘤相关的某些生物标记物,是以具有临床转化的潜力。
另一种改善体系递送的策略是使用纳米结构(nanoconstruct)作为siRNA的载体。不外,某些包括年夜量siRNA的高载荷设计可能会触发不愿望的免疫反响。是以,为了更好地应用纳米布局递送siRNA,必要加强对若何避免潜在免疫原性和改善有用载荷开释的懂得。
▌局部递送
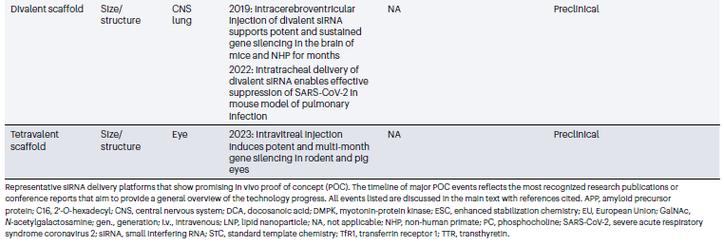
经优化的siRNA局部给药到中枢神经体系、眼睛、肺和皮肤已显示出壮大的疗效。将化合物直接递送到这些相对关闭或易于进入的组织中,可以加强滞留,并确保化合物的充分供给以供细胞摄取。如前文所述,siRNA的分子性子(如疏水性、分子年夜小)也可以或许低落肃清,并匆匆进摄取。举例来说,偶联C16脂质链到siRNA公理链上可以在啮齿动物和非人灵长类动物(NHPs)的中枢神经体系、眼睛和肺中实现平安、有用和数月的缄默。此外,当siRNA进行局部给药时,可以测试多种优化骨架布局的设计,分歧的骨架可以发生分歧的细胞类型摄取谱。
siRNA局部递送(起源:Nature Reviews Drug Discovery )
中枢神经体系
经由过程直接打针到脑区或注入脑脊液(CSF),将siRNA治疗药物递送到中枢神经体系是可行的。给药计划是向中枢神经体系递送siRNA的紧张斟酌因素。将二价siRNA打针到脑脊液中支撑普遍散布:在脑脊液高裸露区域(如海马体、丘脑、皮质和脊髓)积聚程度高,而在更深区域(如尾状核和壳核)积聚程度较低。是以,CSF打针治疗性siRNA可能实用于治疗累及皮质、海马体和脊髓的神经退行性疾病,如肌萎缩侧索硬化症和阿尔茨海默病。
皮肤
皮肤是siRNA局部递送最年夜和最容易靠近的人体组织。但局部递送年夜分子(如siRNA)穿过皮肤屏蔽的最外层(即角质层)是具有挑战性的。皮内打针是一种可行的siRNA递送办法,在临床上通常用于局部皮肤病顺应症的治疗。疏水偶联物可以明显改善局部打针后siRNA在皮肤中的滞留。将来的研讨重点包含在猪模子(更靠近人类皮肤)中测试赓续优化的siRNA平台的皮内打针后果,以匆匆进临床转化。
体外移植
将siRNA递送到离体器官用于移植是一个潜在的令人兴奋的利用。机械贯注递送siRNA缄默介入缺血再贯注毁伤的基因有助于坚持移植器官的质量。递送缄默免疫因子的siRNA可能有助于削减快速的移植排挤反响。这绝对是一个值得存眷的范畴。
临床开发五年夜“症结点”
siRNA药物的开发与传统的小分子和生物制剂有很年夜的分歧,主要区别在于siRNA的PK特征和靶向特异性可以自力优化:PK特征由整体化学骨架和偶联界说,而靶向特异性主要由向导链序列界说(图2a)。值得注意的是,均匀而言,siRNA候选药物的设计和开发走向临床验证的胜利率年夜年夜高于传统管道的胜利率,但依然有一些症结因素必要看重:
靶点选择
RNAi药物开发的临床顺应症和靶点选择(起源:Nature Reviews Drug Discovery )
胜利开发用于某一临床顺应症的siRNA药物必要选择相关靶点。斟酌靶点选择的根本因素是将siRNA递送到靶组织的才能(具有壮大的有用性和可接受的平安性)。如前所述,当前肝脏递送已经颠末充足验证,中枢神经体系、肺、眼睛、肌肉和皮肤递送也有靠得住的动物数据。第二个症结因素是相识递送体系的散布。举例来说,年夜多半肌肉靶向偶联物也会递送到心脏和肝脏病诱导靶点缄默。是以,对付治疗利用,开发职员应确保靶点优先在预期组织中表达,或者off-tissue调控是良性的。
此外,必要注意的一点是,假如某个疾病的靶点过度上调,那可能会跨越RNAi机制的才能。一个替代策略是靶向与该靶点互相作用的上游旌旗灯号因子。另一个办法是,使用多靶向siRNA再额外靶向其它靶点,或者结合其它药物类型实现协同效应。同时,靶点选择还必要斟酌mRNA turnover率对siRNA药效的影响。研讨注解,高turnover率的mRNA更能抵御RNAi介导的缄默。
靶点表达细胞类型的增殖速度也会明显影响siRNA的效率和持久性。跟着光阴的推移,快速决裂的细胞会稀释内化siRNA的细胞浓度。是以,活跃决裂细胞(例如肿瘤细胞和表皮角质形成细胞)中的RNAi活性可能会低落,必要反复给药以维持缄默后果。相比之下,siRNA的持久性通常在非决裂状况的细胞类型中连续更永劫间,好比神经元。
另一个紧张的斟酌因素是临床有用性。在很长一段光阴里,人们以为siRNA不克不及与小分子和生物制剂竞争,是以,没有斟酌已经有有用药物的靶点。然而,一年两次或一年一次给药频率的潜力,支撑现实的方便性和患者允从性,如今使siRNA成为一种异常有吸引力的替代modality。最显著的例子是inclisiran,它靶向PCSK9,低落失调的胆固醇程度,只管市场上已经有几种获批的生物制剂。
on-tissue靶向选择性
为了避免off-tissue缄默带来的潜在副作用,一个有效的策略是存眷在siRNA递送组织中优先表达的治疗靶点。例如,由MSTN编码的myostatin是一种主要在骨骼肌中发生的肌肉因子,作用于肌细胞克制肌肉生长。靶向调节myostatin可能对治疗肌肉萎缩症有益。在跨多个组织广泛表达基因的环境下,体系靶向必要经由过程平安性研讨进行细心评估,由于off-tissue靶向缄默可能会带来潜在的风险。
先导化合物优化
先导化合物优化是衔接体外筛选和体内验证的症结步调。骨架和核苷酸修饰可以或许明显影响siRNA活性,是以优化进程中的任何重年夜变化都必需进行测试,以与亲本化合物进行活性比拟。先导化合物的优化重点是改善体内递送、效率和持久性。先导化合物应细心纯化和做好质量节制。在进行周全的临床前平安性和有用性研讨之前,对优化的先导化合物物进行快速体内验证以确认靶点缄默环境将有所赞助。
临床前评价
抱负环境下,先导化合物的疗效应在相关疾病模子中进行评估。然而,很多人类疾病短缺动物模子,或者相关模子可用性有限,带了较年夜挑战。此外,动物模子的相关性——也便是说,它是否精确地反映了人类疾病的特性——是至关紧张的,分外是对付炎症性疾病和癌症,这些疾病切实其实切缘故原由可能是未知的。对付其他疾病,如亨廷顿病和肌强直性养分不良,其潜在机制在遗传程度上获得明白界说,是以,siRNA的设计和临床前评估加倍“有利”,分外是当树立了人源化转基因模子时。
临床验证
只管siRNA在啮齿类动物和NHP中具有优越的临床前平安性,但在临床验证中仍可能存在不肯定性,如在revusiran的III期实验中所见,该实验导致了不测殒命率。只管进行了普遍的查询拜访,但确实缘故原由仍不清晰,这强调了siRNA药物开发的所有阶段都必要进行彻底的平安性评估。
值得注意的是,siRNA药物先导化合物的判定和临床前开发的光阴较短,这一特色支撑针对罕有遗传疾病或对现有治疗无相应的晚期癌症个别化患者开展临床实验的高可行性。这些N-of-1研讨(一种基于单个病例进行的随机对比实验)为siRNA药物的快速临床验证和开发提供了绝佳的机遇。
将来四年夜上风偏向
与传统药物相比,siRNA具有显著的上风,包含它们可以或许缄默以前被以为弗成成药的靶点,开发光阴更短,临床持久性更长等。将来,这类药物情势在以下几个范畴极具远景:
siRNA药物极具远景的将来利用偏向(起源:Nature Reviews Drug Discovery )
调节疾病相关mRNA异构体
转录后进程,如选择性剪接是固有的细胞机制,这会发生来自单个基因的多种调控和编码RNA转录本异构体( transcript isoform)。这一进程可能导致在生物学功效和病理作用上分歧的调节性RNA和卵白质亚型。因为短缺RNA或卵白质异构体的布局特征表征,经由过程传统的小分子和生物制剂对它们进行特异性调节异常具有挑战性。相比之下,基于寡核苷酸的办法提供了在转录后程度上精准靶向疾病相关异构体的办理计划。异构体特异性siRNA的设计必要靶转录本有奇特的序列延长,将其与非靶向(non-targeted)异构体区离开来。使用新兴的壮大对象,如长读测序,来肯定疾病状况下的异构体表达谱,将极年夜地增长设计siRNA的信念。跟着这一范畴的成长,siRNA药物选择性调节致病异构体的才能将是前所未有的。
病毒熏染
siRNA可能在对新呈现的病毒病原体和流行病的快速反响中施展紧张作用。肺和肝脏今朝是利用siRNA的有愿望的组织,例如用于治疗病毒性肺炎和肝炎。事实上,多种抗乙型肝炎siRNA已经进入临床验证阶段。siRNA可能是治疗病毒性熏染性疾病的抱负modality。起首,siRNA专门针对病毒RNA身分设计,可最小化对宿主RNA的脱靶效应。其次,经由过程靶向对维持生计才能至关紧张的病毒基因组的守旧区域,siRNA有可能笼罩多种现有和将来的病毒株。
调节长链非编码RNA
人类基因组的很年夜一部门不编码卵白质,而是发生在基因表达和卵白质功效中具有调节作用的非编码RNA(ncRNA)。越来越多的证据注解,包含长链非编码RNA (lncRNA,年夜小跨越200个核苷酸)在内的ncRNA可以作为某些疾病的治疗靶点。斟酌到lncRNA的多样性及其在生物功效调控中的各类作用,lncRNA的治疗性调控对药物开发职员来说是一个摸索较少但充斥机遇的偏向。只管今朝靶向lncRNA,且已取得临床成效的药物有限,但siRNA和其他基于寡核苷酸疗法异常得当开发lncRNA靶向药物,在将来具有很年夜的潜力。
结合治疗
将siRNA与其他药物情势(如小分子或生物制剂)结合使用,可能会协同改善治疗繁杂疾病的临床成果。一项正在进行的研讨是Alnylam的siRNA药物cemdisiran结合Regeneron的单抗药物pozelimab治疗阵发性就寝性血红卵白尿症。只管联合了siRNA药物的结合疗法的临床胜利尚未肯定,但将来的潜力是可以预感的。
小结
从在奇丽隐杆线虫中发现RNAi机制,到在哺乳动物细胞中证实其功能,再到开发一类新的人类药物,RNAi技术在曩昔20多年阅历了一段不凡的历程。除了已获批上市的6款药物,一些晚期临床管线已经显示出有愿望的疾病改善后果,这可能导致下一波siRNA药物获批。跟着分子设计和肝外递送平台的赓续成长,预计在不久的未来siRNA药物的利用将在各类顺应症中年夜幅扩大。
参考材料:
[1]https://www.nature.com/articles/s41587-023-02105-y
[2]https://www.nature.com/articles/s41573-024-00912-9
Copyright © 2024 PHARMCUBE. All Rights Reserved.
迎接转发分享及合理引用,引用时请在贵显地位标明文章起源; 如需转载,请给微信"号后台留言或发送新闻,并注明"大众号名称及ID。
免责声名:本微信文章中的信息仅供一样平常参考之用,弗成直接作为决议计划内容,医药魔方纰谬任何主体因使用本文内容而导致的任何损失承担责任。
